Главное
«Икант» (Ycanth, кантаридин) — новый лекарственный препарат, предназначенный для лечения контагиозного моллюска у пациентов в возрасте от 2 лет.
«Икант», разработанный «Веррика фармасьютикалс» (Verrica Pharmaceuticals), дожидается одобрения Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), которое должно принять решение до конца мая 2022 года.
- 25 мая 2022 года FDA отклонило регистрационную заявку «Веррика» ввиду выявленных проблем на площадках «Стерлинг фармасьютикалс сервисиз» (Sterling Pharmaceuticals Services), контрактной производственной организации (CMO), исполняющей заказы на выпуск «Иканта». Обнаруженные недостатки в основном связаны с отдельными операциями со стерильной продукцией, относящимися к обслуживанию других заказчиков, притом что производство «Иканта» не требует стерильности. Тем не менее инспекционные правила FDA не позволяют до момента разрешения любых открытых вопросов с производством одобрять какие-либо лекарственные средства, выпускаемые на мощностях проблемного CMO. «Веррика» продолжит взаимодействовать с регулятором, а также займется поиском альтернативного CMO. Как бы то ни было, биржевые котировки «Веррика» потеряли сразу две трети.
«Икант» станет первым лекарственным средством против контагиозного моллюска, утвержденным американским регулятором. Сейчас лечение этой кожной инфекции осуществляется в режиме офф-лейбл (вне инструкции).
Со временем «Икант» расширит спектр назначений, подключив лечение бородавок и остроконечных кондилом.
Появление препарата «Икант» могло бы состояться много раньше, но «Веррика» уже дважды столкнулась с отказом FDA. Так, в июле 2020 года регулятор отклонил регистрационную заявку, запросив дополнительную информацию, относящуюся к разделу «Химические свойства, процесс производства и контроль качества» (CMC). В сентябре 2021 года регулятор выявил недостатки на площадке контрактной «Стерлинг», не связанные с производством «Иканта».
Согласно оценкам отраслевых обозревателей, спрос на «Икант» в 2026 году перешагнет отметку в четверть миллиарда долларов.
Что такое контагиозный моллюск
Контагиозный моллюск — это широко распространенная вирусная инфекции, поражающая кожу и подкожные слои и проявляющаяся обычно в виде единичных или мелкогрупповых безболезненных пупырчатых телесного цвета папул диаметром 3–5 мм.
Контагиозный моллюск обычно встречается в трех группах населения: дети дошкольного и младшего школьного возраста, сексуально активные подростки или молодые взрослые, дети или взрослые с ослабленным иммунитетом (к примеру, больные ВИЧ или недавно прошедшие химиотерапию). Первые заражаются через тесный физический контакт с другими инфицированными детьми или фомитами (зараженными предметами). Вторые — при половом контакте. Третьи — при физическом или половом контакте и характеризуются более многочисленными, диффузными и крупными поражениями.
Пациенты с атопическим дерматитом подвергаются повышенному риску заражения контагиозным моллюском.
Распространенность контагиозного моллюска в мире среди детей оценивается в пределах 5–11%. Контагиозный моллюск является третьей самой частой кожной инфекцией у детей и входит в пятерку ведущих кожных заболеваний в мире. [1] [2]
Контагиозный моллюск вызывается вирусом контагиозного моллюска (Molluscum contagiosum virus, MCV) — двухцепочечным ДНК-поксвирусом, относящимся к роду Molluscipoxvirus семейства Poxviridae. Идентифицировано минимум 4 подтипа MCV, при этом самым распространенным (75–96% случаев) является 1-й подтип (MCV-1), за ним следует 2-й подтип (MCV-2). Последний ассоциирован с иммунодефицитными состояниями и ВИЧ (у больных ВИЧ встречается в 60% случаев). Инкубационный период MCV составляет от 2 недель до 6 месяцев.
Персистирование поражений, оставляемых без лечения, на протяжении многих недель (обычно 6–9 месяцев, но возможно и до 2 лет) предполагает, что вирус контагиозного моллюска уклоняется от иммунного ответа путем экспрессии ряда белков, препятствующим таковому. Так, например, MC159 и MC160 подавляют апоптоз моллюсковых тел путем ингибирования TRAIL и NF-κB; MC54L предотвращает воспаление посредством связывания интерлейкина 18 (IL-18); MC148 препятствует дифференцировке инфицированных кератиноцитов; MC80R вмешивается в процессы презентации MCV-специфических пептидов и цитотоксичности зараженных клеток; глутатионпероксидаза предотвращает опосредованное лейкоцитами окислительное повреждение. [2] [3]
В отличие от герпесвирусов, которые могут оставаться неактивными в организме в течение месяцев или лет, прежде чем появиться вновь, вирус контагиозного моллюска не сохраняется в организме после исчезновения кожных поражений. Иммунитет к вирусу контагиозного моллюска временный, возможны повторные заражения.
У большинства иммунокомпетентных лиц контагиозный моллюск не требует какого-либо лечения, самостоятельно разрешаясь в течение 6–13 месяц. Для предотвращения вирусного распространения следует избегать сексуальных контактов, вовлекающих пораженные области кожи.
Лечение контагиозного моллюска рекомендовано в следующих случаях: для облегчения зуда или иных симптомов, для устранения косметических проблем (включая социальную стигму, связанную с видимыми поражениями кожи, что отрицательно влияет на качество жизни), для сдерживания самозаражения (при расчесывании, бритье), для предотвращения передачи инфекции другим (особенно при поражении половых органов у сексуально активных людей).
Возможные варианты лечения контагиозного моллюска представлены фармакотерапией (топическими и системными препаратами), хирургическими и другими процедурами. [4] [5] [6] [7] [8]
Среди топических лекарственных средств, доказанно эффективных в лечении контагиозного моллюска: кантаридин (cantharidin), подофиллотоксин (podophyllotoxin), имихимод (imiquimod).
Среди хирургических и других способов лечения контагиозного моллюска: кюретаж (прокалывание центра папулы и выскабливание ее содержимого), удаление сердцевины с помощью экстрактора комедонов, криотерапия.
- Способы лечения контагиозного моллюска с ограниченными доказательствами пользы или сопровождающиеся неблагоприятными последствиями следующие: гидроксид калия (potassium hydroxide), салициловая кислота (salicylic acid), экстракт листьев мирта (myrtle leaf extract), бензоилпероксид (benzoyl peroxide), сочетание повидон-йода (povidone iodine) и салициловой кислоты (salicylic acid), третиноин (tretinoin), гликолевая кислота (glycolic acid), нитрат серебра (silver nitrate), цидофовир (cidofovir), циметидин (cimetidine), интерферон альфа (interferon alfa), лазерные процедуры, пилинг трихлоруксусной кислотой (trichloroacetic acid).
В настоящее время в США нет никакого одобренного FDA способа лечения контагиозного моллюска, и «Икант» должен стать первым таковым.
«Икант»: механизм действия кантаридина
Кантаридин (cantharidin) — химический везикант (кожно-нарывное вещество), выделенный из жуков-нарывников, к которым относится хорошо известная шпанская мушка (Lytta vesicatoria).
После того как кантаридин поглощен липидными мембранами эпидермальных клеток его механизм действия включает активацию или высвобождение эпидермальных сериновых протеаз, разрушающих десмосомальные бляшки (клеточные структуры, участвующие в межклеточной адгезии), что приводит к отслоению тонофиламентов (удерживают клетки вместе). Этот процесс отражается потерей клеточных связей (акантолиз), в конечном итоге вызывая внутриэпидермальные волдыри и воспаление, способствующие отслоению инфицированных кератиноцитов и клиренсу вируса. [1]
Кантаридин широко используется в лечении контагиозного моллюска и бородавок с 1950-х годов. Преимущества кантаридина перед другими методами лечения включают быстрое наступление терапевтического эффекта и отсутствие серьезно выраженных болевых ощущений во время применения. После того как в 1962 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) начало требовать предоставления данных об эффективности одобренных лекарственных препаратов, а производители кантаридина их не предоставили, он был изъят с рынка. В 1997 году кантаридин был вновь представлен в качестве нерасфасованной фармацевтической субстанции, что позволило врачам применять его в клинической практике. Однако неоднозначность FDA-статуса кантаридина приводит к ряду проблем, в том числе с его доступностью. [2]
Несмотря на повсеместное клиническое применение и зарегистрированную безопасность кантаридина, были необходимы надежные клинические испытания, которые окончательно подтвердили бы эффективность и безопасность кантаридина с последующим одобрением его в качестве лекарственного средства против контагиозного моллюска и бородавок.
«Веррика» это сделала первой, предложив топический препарат «Икант» (Ycanth), известный под кодовым обозначением VP-102, содержащий 450 мкл раствора с 0,7 об. % кантаридина и реализованный одноразовым аппликатором с 1-мм наконечником. В состав «Иканта» входит краситель генцианвиолет (кристаллический фиолетовый), облегчающий идентификацию уже обработанных и еще не обработанных поражений.
«Икант»: эффективность и безопасность кантаридина в лечении контагиозного моллюска
Одинаковые по дизайну опорные клинические исследования CAMP-1 (NCT03377790) и CAMP-2 (NCT03377803) фазы III (рандомизированные, двойные слепые, плацебо-контролируемые, многоцентровые) охватили пациентов (n=528) в возрасте 2 лет и старше с контагиозным моллюском.
Возраст участников в основном укладывался в пределы 2–11 лет, мужчин и женщин было поровну, период от постановки диагноза до начала экспериментального лечения составил в среднем 4,2 месяца, приблизительно треть пациентов ранее проходили лечение контагиозного моллюска, число изначальных поражений составило в среднем 21,5.
Испытуемым назначали плацебо или «Икант», которые наносили на все очаги поражения и оставляли на срок 24 часов. Такую процедуру повторяли до 4 раз с интервалом в 21 день.
К первичной конечной точке эффективности лечения контагиозного моллюска, установленной пропорцией пациентов с полным исчезновением всех поддающихся лечению поражений (изначальных и новых) на 84-й день, вышли 46,3% и 54,0% получавших «Икант» участников CAMP-1 и CAMP-2 — против 17,9% и 13,2% в группах плацебо (p<0,0001).
По окончании лечения число поражений (имевшихся и новых) уменьшилось в среднем на 69% и 83% — против его увеличения на 20% и 19% (p<0,05).
Применение «Иканта» отразилось быстрым наступлением терапевтического эффекта: статистически значимое расхождение с группой плацебо наблюдалось уже после первого курса лечения, продолжая улучшаться при последующем использовании препарата.
При объединении результатов клинических испытаний к первичной конечной точке вышли 50% пациентов, лечившихся кантаридином, — против 15,6%, проходивших терапию плацебо (p<0,0001).
По завершении лечения число поражений (имевшихся и новых) уменьшилось в среднем на 76% — против 0,3% (p<0,0001).
Если рассматривать излечение контагиозного моллюска в контексте локализации поражений, результаты следующие: поражения полностью исчезли на голове/шее у 81,8% получавших «Икант» и у 39,6% получавших плацебо, на спине/ягодицах — у 75,2% против 37,4%, на груди/животе — у 71,1% против 37,3%, в паху — у 85,7% против 52,0%, на верхних конечностях — у 66,5% против 33,6%, на нижних конечностях — у 64,0% против 33,3%.
Профиль безопасности «Иканта» характеризовался приемлемой переносимостью: лечение полностью завершили 93,6% пациентов — против 95,4% в контрольных группах. Среди наиболее распространенных нежелательных явлений, возникших в ходе лечения, были побочные реакции по месту применения: везикулы, зуд, боль, эритема, струпья, депигментация, сухость. Все они носили в основном легко-умеренную степень выраженности.
«Икант»: что дальше
«Веррика» намеревается расширить спектр показаний «Иканта», подключив лечение обыкновенных бородавок, остроконечных кондилом (аногенитальных бородавок) и подошвенных бородавок — распространенных кожных инфекций, вызываемых вирусами папилломы человека (ВПЧ).
Так, клиническое испытание COVE-1 (NCT03487549) фазы II проверило кантаридин в лечении обыкновенных бородавок. Применение препарата привело к полному исчезновению кожных поражений у 51,4% пациентов.
Клиническое испытание CARE-1 (NCT03981822) фазы II оценило кантаридин в задаче лечения остроконечных кандилом. Назначение препарата обеспечило полное исчезновение кожных поражений в среднем у 35,1% пациентов, число остроконечных кондилом сократилось в среднем на 76,9%.
Кантаридин
Cantharidin
Фармакологическое действие
Кантаридин — кератолитическое средство, для наружного применения.
Показания
Лечение контагиозного моллюска.
Противопоказания
- Повышенная чувствительность к кантаридину,
- родинки в месте нанесения,
- недиагностированные поражения кожи,
- беременность,
- лактация.
С осторожностью
Сахарный диабет, заболевания периферических сосудов, бородавки в области гениталий и ануса.
Беременность и грудное вскармливание
Применение при беременности
Категория действия на плод по FDA — N.
Адекватных и строго контролируемых исследований по безопасности применения препарата при беременности не проведено. Неизвестно, оказывает ли препарат немедленное или отсроченное негативное воздействие на плод. Применение противопоказано.
Применение в период грудного вскармливания
Специальных исследований по безопасности применения препарата в период грудного вскармливания не проведено. Применение противопоказано.
Способ применения и дозы
Наружно.
Побочные действия
Аллергические реакции.
Классификация
-
Код МКБ 10
-
Категория при беременности по FDA
N
(не классифицировано FDA)
Информация о действующем веществе Кантаридин предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Кантаридин, содержатся в инструкции производителя, прилагаемой к упаковке.
Проведен обзор современных методов лечения инфекции, вызванной контагиозным моллюском. Наиболее подходящий терапевтический подход во многом зависит от клинической ситуации и распространенности контагиозного моллюска. Консервативное лечение с применением различных кремов, мазей, растворов не всегда эффективно и зачастую помогает только при единичных или маленьких вновь появившихся элементах. Ни один из методов наружной терапии не показал достоверных результатов по сравнению с плацебо, но может быть использован как пробный вариант, особенно при категоричном отказе самих пациентов и/или их родителей от механического удаления. К наиболее эффективным методам можно отнести кюретаж, или механическое удаление контагиозного моллюска, который при адекватном местном обезболивании хорошо переносится. Отмечено, что выжидательная тактика не обоснованная, т.к. чаще всего происходит распространение элементов путем аутоакуляции вируса на другие участки кожи за счет травм и трения.
Введение
Контагиозный моллюск – одно из самых распространенных заболеваний кожи и слизистых детей и подростков [1], реже встречающееся у взрослых и протекающее с образованием мелких полушаровидных папул с пупковидным вдавлением в центре. Заболевание обусловлено эпидермотропным вирусом (Molluscum contagiosum virus), который относится к семейству оспенных вирусов (Poxviridae). При исследовании генотипа этого вируса было выявлено четыре типа MCV-1–4, наиболее часто из которых встречается I тип. Последний вызывает 96,6% инфекций. На долю вируса II типа приходятся 3,4% случаев заболеваний, однако не было обнаружено взаимосвязи между типом вируса и морфологией поражения или анатомическим распределением высыпаний [1]. Вирусы III и IV типов встречаются редко и чаще верифицируются у пациентов с иммуннодефицитными состояниями [2].
Контагиозный моллюск редко встречается у детей моложе 1 года, основной же пик заболеваемости приходится на возраст от 2 до 5 лет и связан со случайными прямыми контактами с больными детьми либо передачей инфекции опосредованно через игрушки или предметы обихода. Способ заражения подростков объясняется активностью сексуальных контактов [3, 4]. Мужчины болеют несколько чаще, чем женщины. Распространенность данного заболевания изучена мало, но в последние годы отмечается рост заболеваемости не только в России, но и во многих странах Европы и Америки [5]. При этом выявлено, что у людей с иммуннодефицитными состояниями высыпания более обильные, а заболеваемость гораздо выше. Установлено, что порядка 5–18% всех больных с иммунодефицитом подвержены этому вирусу, а тяжесть инфекции обратно пропорциональна количеству лимфоцитов CD4 [6]. У пациентов с различными хроническими заболеваниями кожи, сопровождающимися сухостью (например, атопический дерматит и экзема), вирус контагиозного моллюска активизируется, иногда вызывая генерализацию процесса [5]. Более развернутая клиническая картина по количеству высыпных элементов, площади пораженной кожи и устойчивости инфекции также отмечается у пациентов, получающих преднизон и метотрексат. Кроме того, описаны случаи активизации вируса в виде диссеминации контагиозного моллюска при лечении экземы, атопического дерматита, витилиго мазью такролимус 1% [7, 8].
Возбудитель передается опосредованным путем через постельное и нательное белье, полотенца, посуду, игрушки, мочалки, при контактных видах спорта, массаже, посещении бассейна, принятии общих ванн, либо прямым контактным способом во время половых контактов взрослых и подростков [1, 9, 10]. Инкубационный период обычно составляет 2–7 недель, но может удлиняться до 6 месяцев. Это связано с тем, что, хотя вирусные частицы первично локализуются в базальном слое, репликация вирусной ДНК и образование новых вирусных частиц не происходят до тех пор, пока не будут задействованы шиповатый и зернистый слои эпидермиса. Вирус контагиозного моллюска не имеет латентного периода и не существует в организме постоянно как вирус герпеса. Для отсутствия формирования стойкого иммунного ответа важно то, что он вырабатывает вирус-специфические белки, которые помогают ему избегать агрессии со стороны иммунной системы. Таким образом, если после излечения у пациента снова появились очаги контагиозного моллюска, значит, он снова вступил в контакт с инфицированным человеком или объектом.
Высыпания можно обнаружить на любом участке кожи, но у детей очаги контагиозного моллюска обычно возникают на груди, руках, туловище, ногах и лице. Множественные элементы также могут развиваться в подмышечных и паховых областях. Крайне редко встречаются единичные элементы на слизистых оболочках губ, век, языка и слизистой рта. У взрослых контагиозный моллюск чаще всего ограничен областями промежности, гениталий, нижней части живота или ягодиц.
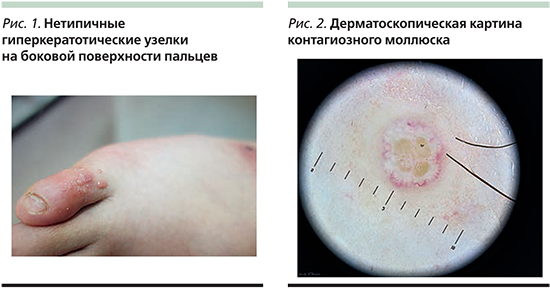
Клинически на неизмененной коже выявляются изолированные полушаровидные с жемчужным блеском узелки величиной от 1–3 до 5–10 мм в диаметре, имеющие цвет нормальной кожи или бледно-розовый, чаще всего располагающиеся группами, но могут встречаться и в виде единичного элемента. В центре некоторых элементов наблюдается пупкообразное вдавление, заполненное роговыми массами. При вскрытии и надавливании из центрального углубления выделяется белесое вещество творожистой консистенции, состоящее из ороговевших клеток эпидермиса и овоидных телец. Как правило, высыпания не беспокоят, но иногда они могут сопровождаться зудом, экзематозной реакцией и за счет травмы начинают появляться новые очаги, что ведет к распространению заболевания. В клинической практике надо также учитывать, что у 10% пациентов с контагиозным моллюском встречаются атипичные высыпания, например, на тыльной или боковой поверхностях стоп и кистей, они чаще всего выглядят как сухие гиперкератотические узелки (рис. 1), а в ряде случаев в нижней трети лица и на шее могут имитировать акнеформные элементы.
Пока элементы существуют на коже, пациент считается заразным для окружающих. Появление выраженной воспалительной реакции отдельных элементов может говорить о последующей элиминации вируса или же о его травматизации и последующем распространении. Как правило, процесс протекает без осложнений заболевания, но иногда могут быть такие, как присоединение бактериальной инфекции (требует назначения антибактериальных препаратов), рубцевание (чаще встречается при постоянной травматизации ряда элементов или после недостаточно корректного удаления элементов), конъюнктивит или кератит (при наличии элементов на лице в области глаз). В последнем случае пациенты могут ощущать боль, отмечать покраснение и отечность, а также болезненность, слезотечение и светочувствительность глаз. Еще одно редкое осложнение контагиозного моллюска – рожистое воспаление – встречается у пациентов, инфицированных вирусом иммунодефицита человека [11]. Диагноз контагиозного моллюска чаще всего устанавливается при простом осмотре кожных покровов, иногда приходится прибегать к дерматоскопии образований, в ряде случаев проводят микроскопию или даже гистологическое исследование элементов.
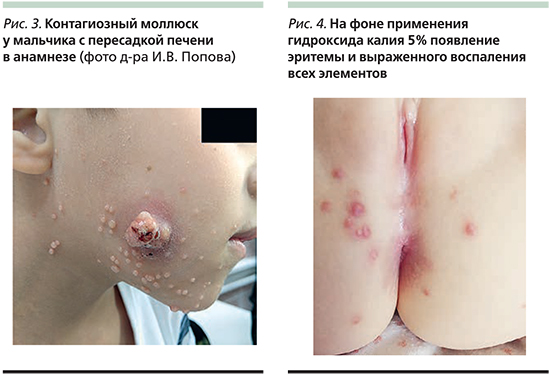
При дерматоскопии контагиозного моллюска можно выявить следующие особенности (рис. 2):
- папула с углублением в центральной области, в которой также могут наблюдаться оранжевые или желтоватые роговые массы;
- гомогенные белесовато-розовые глобулы в центральной области (при сильном нажатии белые);
- множественные линейные или извитые сосуды по периферии очага.
Дифференциальный диагноз проводят с бородавками, папилломами, ветряной оспой, эпидермальной кистой, гиперплазией сальной железы, дерматофибромами, бородавчатым красным плоским лишаем, пиогенной гранулемой, в редких случаях – с раком кожи.
Лечение
Терапевтические возможности лечения контагиозного моллюска включают применение различных наружных средств, механические способы, электрокоагуляцию, крио- или лазерное удаление, пероральные лекарственные средства. Но часто одного сеанса терапии не хватает из-за недостаточной активности препаратов, рецидива или появления новых элементов.
Консервативное лечение с применением различных кремов, мазей, растворов (имиквимод, ретиноиды, 5–10%-ные растворы гидроксида калия и др.) не всегда эффективны и зачастую помогают только при единичных или маленьких вновь появившихся элементах. Спонтанное излечение наблюдается чрезвычайно редко (при единичных элементах) и происходит в период до 18 месяцев после появления, описаны единичные случаи саморазрешения элементов в течение 4 лет.
В большинстве случаев родители детей выбирают выжидательную тактику и не лечат контагиозный моллюск, что чаще всего приводит к распространению элементов и заражению других людей, находящихся в окружении. Выжидательная тактика особенно опасна для людей с различными иммуннодефицитными состояниями, т.к. упущенное время может приводить к масштабному распространению процесса с последующей необходимостью применения общего наркоза для удаления элементов [11]. В некоторых случаях специалисты предлагают при лечении совмещать несколько способов, т.к. не всегда представляется возможным очистить кожу от контагиозного моллюска, применяя только один метод лечения [12].
Наиболее подходящий терапевтический подход во многом зависит от клинической ситуации и распространенности контагиозного моллюска. Для здоровых детей основная цель – ограничить дискомфорт, травматизацию и привести к ограничению распространения. Для взрослых, чаще всего готовых к лечению, эффективны криотерапия, электрокоагуляция или кюретаж отдельных элементов, и они их хорошо переносят.
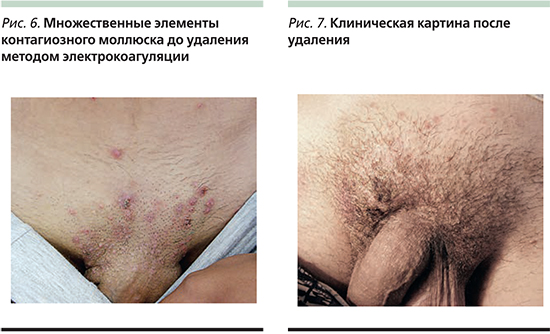
У лиц с ослабленным иммунитетом высыпания при контагиозном моллюске могут быть весьма обширными и трудно поддающимися лечению (рис. 3). Цель может заключаться в лечении самых больших, раздраженных или сливающихся высыпаний. В тяжелых случаях этим пациентам могут потребоваться более агрессивная деструкция лазером, противовирусная терапия или их комбинация [13]. Эффективная антиретровирусная терапия пациентов с синдромом приобретенного иммунодефицита делает терапию контагиозного моллюска намного более эффективной.
Топические препараты, используемые в терапии заболевания, перечислены ниже.
Гидроксид калия (Молютрекс 5%, Молюсдерм 10%) – средство в виде раствора. Применяется местно для лечения контагиозного моллюска, разрушает клетки кожи, инфицированные вирусом, позволяя выработать адекватный иммунный ответ. Раствор наносят 2 раза в день на каждый элемент, добиваясь появления признаков воспаления и разрешения очагов после этого в течение нескольких недель. Обработку прерывают на несколько недель сразу при появлении воспаления (рис. 4, 5). Если при применении в течение 14 дней признаков воспаления нет, стоит делать перерыв и препарат не использовать. К побочным эффектам данных препаратов относят легкое жжение, покраснение, зуд, которые обычно уходят через несколько минут после нанесения лекарства на кожу [14, 15]. В Кокрановской базе данных опубликован обзор результатов исследования, в которых изучалось влияние нескольких наружных, системных и гомеопатических средств [16]. Среди полученных результатов исследователи не обнаружили статистически значимых различий между лечением плацебо и терапией гидроксидом калия или между лечением плацебо и различными гомеопатическими препаратами.
Имиквимод (Алдара, Кераворт, Вартоцид) – это крем, используемый для обработки больших зон или крупных скоплений элементов. Лечебный эффект препарата обусловлен его стимулирующим воздействием на иммунную систему. Крем наносится 3 раза в неделю на ночь, а утром смывается через 6–10 часов. Требуется несколько недель терапии для появления результата. Общие побочные эффекты имиквимода включают шелушение кожи, образование выраженных корок, покраснение и отек, ощущение жжения и зуда, иногда головные боли. Данные осложнения обычно разрешаются в течение 2 недель после прекращения лечения и дополнительной коррекции не требуют. Позднее установлено, что имиквимод не эффективен в виде монотерапии контагиозного моллюска и применяется только в комбинации с другими методами лечения [16–21].
Бензоил пероксид (Базирон АС, Продерм, Десквам, Экларан) – крем или гель. Его наносят тонким слоем на элементы 1 или 2 раза в день после душа или умывания на сухую чистую кожу. Бензоил пероксид может усилить чувствительность к солнечному свету, поэтому следует избегать чрезмерного воздействия солнечного и ультрафиолетового света или использовать солнцезащитный крем. К побочным эффектам бензоил пероксида относят покраснение и сухость, шелушение кожи, жжение и зуд в местах нанесения препарата. Обычно не требуется дополнительных способов лечения, элементы полностью разрешаются самостоятельно после завершения терапии.
Третиноин (Ретин-А, Весаноид, Локацид) доступен в виде жидкости и крема, которые применяются 1 или 2 раза в день на отдельные элементы. Как и в случае с бензоил пероксидом, третиноин может усилить чувствительность кожи к солнечному свету и ультрафиолетовому излучению. Наиболее распространенные побочные эффекты третиноина – это легкое раздражение и жжение кожи. С момента начала лечения до улучшения обычно проходит более 2 недель. В случаях нанесения третиноина на обширные участки кожи он может вызывать выраженную экзематизацию и воспаление окружающей кожи, что, наоборот, может приводить к аутоакуляции (самораспространение).
Кантаридин относится к раздражающим средствам (низкомолекулярный токсин), при нанесении на кожу через 2–5 часов вызывает образование волдырей, пузырьков, и пока они целые, боли не отмечается, после же вскрытия возникают раздражение, жжение, боль. Чаще всего используется в сочетании с имиквимодом.
В ряде исследований показана высокая эффективность такой комбинации. При этом первично назначается нанесение только на несколько элементов, чтобы проверить реакцию пациента на терапию [22, 23]. Кантаридин не одобрен Управлением по контролю за продуктами и лекарствами США, но долгое время американскими дерматологами использовался как безопасный и эффективный препарат [24, 25]. Различные виды кислот (би- и трихлоруксусная, салициловая, молочная, гликолевая) рекомендуют применять только под контролем специалиста, т.к. самостоятельное нанесение нередко приводит к рубцеванию и пигментации (рис. 3), помимо этого во многих исследованиях показано, что эффективны достаточно высокопроцентные растворы кислот – от 15% [26].
Антивирусные препараты для перорального приема (цидофовир, ритонавир). Предположительно противовирусные препараты могут препятствовать репликации вируса контагиозного моллюска. Из-за их дороговизны, длительной схемы лечения и возможных побочных действий их относят к препаратам выбора только для пациентов с ослабленным иммунитетом [27].
В некоторых исследованиях показано, что постепенное удаление контагиозного моллюска возможно путем приема циметидина, говорится о возможности его применения детьми, т.к. он безопасен, безболезнен и хорошо переносится, в то же время данных о его применении при контагиозном моллюске совсем мало, помимо этого препарат предназначен в первую очередь для лечения язвенной болезни желудка и, как предполагается, его действие при инфекции, вызванной контагиозным моллюском, опосредованно за счет влияния на иммунную систему.
В России допустимый возраст применения данного препарата от 14 лет, что делает невозможным его применение в педиатрической практике [28].
Управление по контролю за продуктами и лекарствами США не одобрило ни одного из местных или пероральных средств лечения контагиозного моллюска.
Другие методы лечения всегда должны выполняться квалифицированным специалистом.
Криотерапия включает замораживание очагов жидким азотом для их удаления. Каждый элемент замораживается в течение 5–10 секунд. Некоторые авторы с успехом применяют криодеструкцию для удаления контагиозного моллюска [29]. Обычно требуется несколько сеансов криотерапии, прежде чем все элементы полностью уйдут. А между процедурами рекомендуется делать перерыв не менее 10 дней, чаще – 2–3 недели, поэтому данный метод может увеличить сроки лечения.
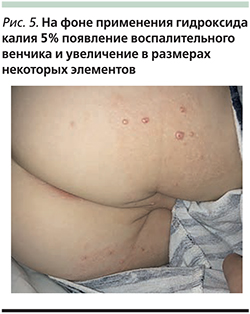
Электрокоагуляция (диатермокоагуляция) использует тепло для удаления элементов. Перед удалением применяют местную анестезию в виде аппликаций растворов, кремов или мазей или местных инъекций анестетиками (лидокаин, прокаин или ультракаин). При обширных высыпаниях данный метод, как и любой другой метод деструкции, болезненен даже при применении местного обезболивания (рис. 6, 7).
Механическое удаление проводится острой кюреткой (малой ложкой Фолькмана) или пинцетом с тупыми концами. После выдавливания очаги обрабатывают 5%-ным спиртовым раствором йода. Как и при электрокоагуляции, до удаления используют местную анестезию [30, 31].
Лазерная деструкция – относительно новый тип лечения контагиозного моллюска. Во время и после процедуры может наблюдаться дискомфорт в зоне удаления, жжение, изменение цвета кожи. Обычно эти проявления уходят в течение нескольких недель. Чаще всего одной процедуры оказывается недостаточно [32–36].
Повторное обследование после любого способа терапии рекомендуется проводить через 2–4 недели, и, как правило, требуется повторное лечение. Если элементы плохо поддаются той или иной терапии, рекомендовано рассматривать комбинированную терапию несколькими методами [13]. Рецидивы возникают у 35% пациентов после первого избавления от всех элементов и могут представлять собой реинфекцию, обострение продолжающегося заболевания или новые поражения, возникающие после длительного инкубационного периода.
В результате поисков наиболее действенного лечения контагиозного моллюска в отношении детей проведено проспективное рандомизированное исследование, в котором сравнивались эффективность и побочные эффекты четырех ранее признанных методов лечения контагиозного моллюска у 124 детей [37]. В первой группе применяли кюретаж, во второй – кантаридин, в третей – комбинацию салициловой и молочной кислот, в четвертой – имиквимод. Установлено, что кюретаж – наиболее эффективный метод лечения, имеет самый низкий уровень побочных эффектов, но требует адекватной анестезии. Кантаридин менее эффективен, как правило, хорошо переносится, но имеет умеренные осложнения в виде пузырьковых высыпаний. Комбинация салициловой и молочной кислот вызывает слишком сильное раздражение, поэтому плохо переносится пациентами детского возраста. Имиквимод вообще не показал эффективности в отношении контагиозного моллюска в составе монотерапии и не рекомендован авторами исследования к применению.
Заключение
Исходя из проведенного обзора существующих методов лечения, можно сделать следующие выводы:
- Кюретаж, или механическое удаление контагиозного моллюска, наиболее эффективен для всех возрастных групп пациентов, а при адекватном местном обезболивании хорошо переносится.
- Пациентам с иммунодефицитами рекомендовано применение комбинации методов, чаще это лазерное удаление параллельно с адекватной противовирусной терапией.
- Ни один из методов наружной терапии не показал достоверных результатов по сравнению с плацебо, но может быть использован как пробный вариант, особенно при категоричном отказе самих пациентов и/или их родителей от механического удаления, чтобы не провоцировать появления новых элементов, или же для обработки мелких только появившихся элементов диаметром до 2 мм, пока не имеющих казеозного содержимого.
- Выжидательная тактика не обоснованна, т.к. чаще всего происходит распространение элементов путем аутоакуляции вируса на другие участки кожи за счет травм и трения.
1. Brown J., Janniger C.K., Schwartz R.A., Silverberg N.B.Childhood molluscum ontagiosum. Int J Dermatol. 2006;45(2):93–9. Doi: 10.1111/j.1365-4632.2006.02737.x.
2. Scholz J., Rosen-Wolff A., Bugert J., et al. Epidemiology of molluscum contagiosum using genetic analysis of the viral DNA. J Med Virol. 1989;27(2):87–90.
3. Laxmisha C., Thappa D.M., Jaisankar T.J. Clinical profile of molluscum contagiosum in children versus adults. Dermatol Online J. 2003;9(5):1.
4. Dohil M.A., Lin P., Lee J., et al. The epidemiology of molluscum contagiosum in children. J Am Acad Dermatol. 2006 Jan. 54(1):47–54. Doi: 10.1016/j.jaad.2005.08.035.
5. Berger E.M., Orlow S.J., Patel R.R., Schaffer J.V. Experience with Molluscum Contagiosum and associated Inflammatory Reactions in pediatric dermatology practice: The bump That Rashes. Arch. Dermatol. 2012;148(11):1257–64. Doi: 10.1001/archdermatol.2012.2414.
6. Zichichi L., Maniscalco M., The challenges of neglected STI: Molluscum contagiosum. G. Ital. Dermatol. Venereol. 2012;147(5):447–53.
7. Ahn B.K., Kim B.D., Lee S.J., Lee S.H. Molluscum contagiosum infection during the treatment of vitiligo with tacrolimus ointment. J Am Acad Dermatol. 2005;52(3 Pt 1):532–33.
8. Fery-Blanco C., Pelletier F., Humbert P., Aubin F. Disseminated molluscum contagiosum during topical treatment of atopic dermatitis with tacrolimus: efficacy of cidofovir. Ann Dermatol Venereol. 2007;134 (5 Pt 1):457–59.
9. Choong K.Y., Roberts L.J. Molluscum contagiosum, swimming and bathing: a clinical analysis. Australas J Dermatol. 1999;40(2):89–92,
10. Connell C.O., Oranje A., Van Gysel D., Silverberg N.B. Congenital molluscum contagiosum: report of four cases and review of the literature. Pediatr Dermatol. 2008;25(5):553–56. Doi:10.1111/j.1525-1470.2008.00730.x.
11. Freeman C.L., Moriarty A.T. Molluscum contagiosum presenting as cellulitis in an AIDS patient: cytologic and ultrastructural features. Diagn Cytopathol. 199;12(4):345–49.
12. Rush J., Dinulos J.G. Childhood skin and soft tissue infections: new discoveries and guidelines regarding the management of bacterial soft tissue infections, molluscum contagiosum, and warts. Curr Opin Pediatr. 2016;28(2):250–57. Doi: 10.1097/MOP.0000000000000334.
13. Nguyen H.P., Franz E., Stiegel K.R., et al. Treatment of molluscum contagiosum in adult, pediatric, and immunodeficient populations. J Cutan Med Surg. 2014;18(5):299–306.
14. Romiti R., Ribeiro A.P., Grinblat B.M., et al. Treatment of molluscum contagiosum with potassium hydroxide: a clinical approach in 35 children. Pediatr Dermatol. 1999;16(3):228–31.
15. Romiti R., Ribeiro A.P., Romiti N. Evaluation of the effectiveness of 5% potassium hydroxide for the treatment of molluscum contagiosum. Pediatr Dermatol. 2000;17(6):495.
16. Van der Wouden J.C., van der Sande R., van Suijlekom-Smit L.W., Berger M., Butler C., Koning S. Interventions for cutaneous molluscum contagiosum. Cochrane Database Syst Rev. 2009;7(4):CD004767.
17. Katz K.A., Swetman G.L. Imiquimod, molluscum, and the need for a better “best pharmaceuticals for children” act. Pediatrics. 2013;132(1):1–3. Doi: 10.1542/peds.2013-0116.
18. Katz K.A. Dermatologists, imiquimod, and treatment of molluscum contagiosum in children: righting wrongs. JAMA Dermatol. 2015;151(2):125–26. doi:10.1001/jamadermatol.2014.3335.
19. Katz K.A. Imiquimod is not an effective drug for molluscum contagiosum. Lancet Infect Dis. 2014;14(5):372–73. Doi:10.1016/S1473-3099(14)70728-5
20. Guzman A.K., Schairer D.O., Garelik J.L., Cohen S.R.Safety and efficacy of topical cantharidin for the treatment of pediatric molluscum contagiosum: a prospective, randomized, double-blind, placebo-controlled pilot trial. Int J Dermatol. 2018;57(8):1001–6.
21. Go U., Nishimura-Yagi M., Miyata K., Mitsuishi T. Efficacy of combination therapies of topical 5% imiquimod and liquid nitrogen for penile molluscum contagiosum. J Dermatol. 2018 Apr 18. Doi: 10.1111/1346-8138.14319.
22. Ross G.L, Orchard D.C. Combination topical treatment of molluscum contagiosum with cantharidin and imiquimod 5% in children: a case series of 16 patients. Australas J Dermatol. 2004;45(2):100–2. Doi 10.1111/j.1440-0960.2004.00066.x.
23. Mathes E.F., Frieden I.J. Treatment of molluscum contagiosum with cantharidin: a practical approach. Pediatr Ann. 2010;39(3):124–28, 130. https://doi.org/10.3928/00904481-20100223-03
24. Silverberg N.B., Sidbury R., Mancini A.J. Childhood molluscum contagiosum: experience with cantharidin therapy in 300 patients. J Am Acad Dermatol. 2000;43(3):503–7. Doi: 10.1067/mjd.2000.106370.
25. Cathcart S., Coloe J., Morrell D.S. Parental satisfaction, efficacy, and adverse events in 54 patients treated with cantharidin for molluscum contagiosum infection. Clin Pediatr (Phila). 2009;48(2):161–65. Doi:10.1177/0009922808326085.
26. Potassium hydroxide 5% for the treatment of molluscum contagiosum. Drug Ther Bull. 2014;52(10):118–20. Doi: 10.1136/dtb.2014.10.0285.
27. Hicks C.B., Myers S.A., Giner J. Resolution of intractable molluscum contagiosum in a human immunodeficiency virus infected patient after institution of anti-retroviral therapy with ritonavir. Clin Infect Dis 1997;24:1023–25.
28. Dohil M., Prendiville J.S. Treatment of molluscum contagiosum with oral cimetidine: clinical experience in 13 patients. Pediatr Dermatol. 1996;13:310–12. Doi: 10.1111/j.1525-1470.1996. tb01247.x.
29. Zimmerman E.E., Crawford P. Cutaneous cryosurgery. Am. Fam. Physician. 2012;86(12):1118–24.
30. Martin-Garcia R.F., Garcia M.E., Rosado A. Modified curettage technique for molluscum contagiosum. Pediatr Dermatol. 2007;24(2):192–94.
31. Simonart T, De Maertelaer V. Curettage treatment for molluscum contagiosum: a follow-up survey study. Br J Dermatol. 2008;159(5):1144–47. http://reference.medscape.com/medline/abstract/17461823
32. Binder B., Weger W., Komericki P., Kopera D. Treatment of molluscum contagiosum with a pulsed dye laser: Pilot study with 19 children. J Dtsch Dermatol Ges. 2008;6(2):121–25.
33. Chatproedprai S., Suwannakarn K., Wananukul S., et al. Efficacy of pulsed dyed laser (585 nm) in the treatment of molluscum contagiosum subtype 1. Southeast Asian J Trop Med Public Health. 2007;38(5):849–54.
34. Hammes S., Greve B., Raulin C. Molluscum contagiosum: treatment with pulsed dye laser. Hautarzt. 2001;52(1):38–42.
35. Hughes P.S. Treatment of molluscum contagiosum with the 585-nm pulsed dye laser. Dermatol Surg. 1998;24(2):229–30. Doi: 10.1111/j.1524-4725.1998.tb04141.x.
36. Michel J.L. Treatment of molluscum contagiosum with 585 nm collagen remodeling pulsed dye laser. Eur J Dermatol. 2004;14(2):103–6.
37. Hanna D., Hatami A., Powell J., et al. A prospective randomized trial comparing the efficacy and adverse effects of four recognized treatments of molluscum contagiosum in children. Pediatr Dermatol. 2006;23(6):574–79.
Автор для связи: Н.С. Сирмайс – к.м.н., доцент кафедры дерматовенерологии и косметологии, Институт повышения квалификации ФМБА, Москва, Россия; e-mail: Natsirmais@mail.ru
Generic name: Cantharidin [ kan-THAR-e-din ]
Medically reviewed by Drugs.com. Last updated on Apr 10, 2023.
Uses of Cantharidin:
- It is used to get rid of warts.
What do I need to tell my doctor BEFORE I take Cantharidin?
- If you have an allergy to cantharidin or any other part of cantharidin.
- If you are allergic to cantharidin; any part of cantharidin; or any other drugs, foods, or substances. Tell your doctor about the allergy and
what signs you had. - If you have a type of wart called mosaic wart.
- If skin around the treated area is swollen or irritated.
- If you have any blood flow problems, talk with your doctor.
- If you have high blood sugar (diabetes).
- If your skin has birthmarks, moles, bleeding warts, or warts with hair growth. Do not use cantharidin on these areas.
- If you drink alcohol. You must avoid drinking alcohol for several hours after treatment.
- If you are pregnant or may be pregnant. Do not use cantharidin if you are pregnant.
- If you are breast-feeding. Do not take cantharidin if you are breast-feeding.
This is not a list of all drugs or health problems that interact with cantharidin.
Tell your doctor and pharmacist about all of your drugs (prescription or OTC, natural products, vitamins) and health problems. You must check
to make sure that it is safe for you to take cantharidin with all of your drugs and health problems. Do not start, stop, or change the dose of
any drug without checking with your doctor.
What are some things I need to know or do while I take Cantharidin?
- Tell all of your health care providers that you take cantharidin. This includes your doctors, nurses, pharmacists, and dentists.
- Talk with your doctor before you drink alcohol.
- Talk with your doctor before you use other drugs or products on your skin.
How is this medicine (Cantharidin) best taken?
Use cantharidin as ordered by your doctor. Read all information given to you. Follow all instructions closely.
- Your doctor or other healthcare provider will put on the skin.
- Follow what your doctor has told you to do.
What do I do if I miss a dose?
- Call the doctor for an office visit.
What are some side effects that I need to call my doctor about right away?
WARNING/CAUTION: Even though it may be rare, some people may have very bad and sometimes deadly side effects when taking a drug. Tell your
doctor or get medical help right away if you have any of the following signs or symptoms that may be related to a very bad side effect:
- Signs of an allergic reaction, like rash; hives; itching; red, swollen, blistered, or peeling skin with or without fever; wheezing;
tightness in the chest or throat; trouble breathing, swallowing, or talking; unusual hoarseness; or swelling of the mouth, face, lips, tongue,
or throat. - Very bad skin irritation.
What are some other side effects of Cantharidin?
All drugs may cause side effects. However, many people have no side effects or only have minor side effects. Call your doctor or get medical
help if any of these side effects or any other side effects bother you or do not go away:
- Skin irritation.
- Blistering.
- Short-term pain after use.
- Change in color of skin where drug is used.
These are not all of the side effects that may occur. If you have questions about side effects, call your doctor. Call your doctor for medical
advice about side effects.
You may report side effects to the FDA at 1-800-332-1088. You may also report side effects at https://www.fda.gov/medwatch.
If OVERDOSE is suspected:
If you think there has been an overdose, call your poison control center or get medical care right away. Be ready to tell or show what was
taken, how much, and when it happened.
How do I store and/or throw out Cantharidin?
- This medicine will be given in a hospital or doctor’s office. You will not store it at home.
Consumer Information Use and Disclaimer
- If your symptoms or health problems do not get better or if they become worse, call your doctor.
- Do not share your drugs with others and do not take anyone else’s drugs.
- Keep all drugs in a safe place. Keep all drugs out of the reach of children and pets.
- Throw away unused or expired drugs. Do not flush down a toilet or pour down a drain unless you are told to do so. Check with your
pharmacist if you have questions about the best way to throw out drugs. There may be drug take-back programs in your area. - Some drugs may have another patient information leaflet. Check with your pharmacist. If you have any questions about cantharidin, please talk
with your doctor, nurse, pharmacist, or other health care provider. - If you think there has been an overdose, call your poison control center or get medical care right away. Be ready to tell or show what was
taken, how much, and when it happened.
Further information
Always consult your healthcare provider to ensure the information displayed on this page applies to your personal circumstances.
Medical Disclaimer
Занидип®-Рекордати (Zanidip®-Recordati) инструкция по применению
📜 Инструкция по применению Занидип®-Рекордати
💊 Состав препарата Занидип®-Рекордати
✅ Применение препарата Занидип®-Рекордати
📅 Условия хранения Занидип®-Рекордати
⏳ Срок годности Занидип®-Рекордати
Описание лекарственного препарата
Занидип®-Рекордати
(Zanidip®-Recordati)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2023
года, дата обновления: 2023.03.31
Владелец регистрационного удостоверения:
Код ATX:
C08CA13
(Лерканидипин)
Лекарственные формы
| Занидип®-Рекордати |
Таб., покр. пленочной оболочкой, 10 мг: 7, 10, 14, 15, 20, 21, 25, 28, 30, 35, 40, 42, 45, 49, 50, 56, 60, 70, 75, 80, 84, 90, 98, 100, 105, 112, 120, 125, 140, 150, 168, 175, 180, 196 или 210 шт. рег. №: ЛП-000705 |
|
|
Таб., покр. пленочной оболочкой, 20 мг: 7, 10, 14, 15, 20, 21, 25, 28, 30, 35, 40, 42, 45, 49, 50, 56, 60, 70, 75, 80, 84, 90, 98, 100, 105, 112, 120, 125, 140, 150, 168, 175, 180, 196 или 210 шт. рег. №: ЛП-000705 |
Форма выпуска, упаковка и состав
препарата Занидип®-Рекордати
Таблетки, покрытые пленочной оболочкой, светло-желтого цвета, круглые, двояковыпуклые, с риской на одной стороне, на изломе светло-желтого цвета.
Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая (тип 101), карбоксиметилкрахмал натрия (тип A), повидон-К30, магния стеарат.
Состав оболочки: готовое пленочное покрытие [гипромеллоза, тальк, титана диоксид (E171), макрогол-6000, краситель железа оксид желтый (E172)].
7 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
10 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
14 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
15 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
20 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
25 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
28 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
30 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
Таблетки, покрытые пленочной оболочкой, от розового до темно-розового цвета, круглые, двояковыпуклые, с риской на одной стороне, на изломе светло-желтого цвета.
Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая (тип 101), карбоксиметилкрахмал натрия (тип A), повидон-К30, магния стеарат.
Состав оболочки: готовое пленочное покрытие [гипромеллоза, тальк, титана диоксид (E171), макрогол-6000, краситель железа оксид красный (E172)].
7 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
10 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
14 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
15 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
20 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
25 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
28 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
30 шт. — блистеры (1, 2, 3, 4, 5, 6, 7) — пачки картонные.
Фармако-терапевтическая группа:
БМКК
Фармакологическое действие
Лерканидипин — высокоселективный блокатор кальциевых каналов группы дигидропиридина. Блокирует трансмембранный ток ионов кальция в гладкомышечные клетки сосудистой стенки и кардиомиоциты. Антигипертензивный эффект лерканидипина обусловлен прямым релаксирующим влиянием на гладкую мускулатуру сосудов, что снижает общее периферическое сопротивление.
Несмотря на короткий T1/2, лерканидипин обладает длительной антигипертензивной активностью, обусловленной высоким коэффициентом мембранного распределения. Благодаря высокой селективности в отношении гладкомышечных клеток сосудистой стенки лерканидипин лишен отрицательных инотропных эффектов.
Расширение сосудов, вызванное приемом препарата Занидип®-Рекордати, происходит постепенно, поэтому острая артериальная гипотензия с рефлекторной тахикардией у пациентов с артериальной гипертензией наблюдается редко. Антигипертензивная активность лерканидипина, как и других асимметричных 1,4-дигидропиридинов, обусловлена его (S)-энантиомером. Эффективность и безопасность лерканидипина в дозе 10-20 мг 1 раз/сут оценивалась в двойных слепых плацебо-контролируемых клинических исследованиях, с участием пациентов с мягкой, умеренной и тяжелой артериальной гипертензией, а также с изолированной систолической гипертензией (в т.ч. у пожилых пациентов и пациентов с сахарным диабетом), получавших лерканидипин, как в монотерапии, так и в комбинации с ингибиторами АПФ, диуретиками или бета-адреноблокаторами.
У пациентов с тяжелой артериальной гипертензией (среднее диастолическое АД — 114.5±3.7 мм рт.ст.), АД нормализовалось у 56% при приеме по 10 мг препарата Занидип®-Рекордати 1 раз/сут и у 40% при приеме препарата по 20 мг. А у пациентов с изолированной систолической гипертензией систолическое АД эффективно снизилось с исходных значений 172.6±5.6 мм рт.ст. до 140.2±8.7 мм рт.ст.
Клинические исследования в педиатрической популяции не проводились.
Фармакокинетика
Всасывание
Лерканидипин полностью всасывается после приема внутрь. Cmax в плазме крови достигается через 1.5-3 ч и составляет 3.3±2.09 нг/мл и 7.66±5.90 нг/мл после приема 10 и 20 мг лерканидипина соответственно.
Оба энантиомера лерканидипина демонстрируют сходный фармакокинетический профиль: имеют одинаковое Тmax, одинаковый Т1/2; значения Сmax и AUC в 1.2 раза выше для (-)S-энантиомера. Взаимопревращения энантиомеров в условиях in vivo не наблюдалось.
В связи со значительным метаболизмом при «первом прохождении» через печень абсолютная биодоступность лерканидипина у пациентов при приеме внутрь после еды составляет приблизительно 10%; в то же время при приеме лерканидипина здоровыми добровольцами натощак биодоступность уменьшается на 1/3.
При приеме лерканидипина не позднее 2 ч после приема жирной пищи его биодоступность увеличивается в 4 раза. В связи с этим препарат Занидип®-Рекордати следует принимать до еды.
Распределение
Распределение из плазмы крови в ткани и органы происходит быстро и обширно. Связывание с белками плазмы крови превышает 98%. У пациентов с тяжелой почечной и/или печеночной недостаточностью из-за снижения концентрации белка в плазме крови, сводная фракция лерканидипина может увеличиваться.
Метаболизм
Лерканидипин интенсивно метаболизируется с участием изофермента CYP3A4; неизмененное действующее вещество не обнаруживается ни в моче, ни в кале. Препарат в основном превращается в неактивные метаболиты.
Исследования in vitro с микросомами печени человека показали, что лерканидипин в некоторой степени ингибирует ферменты CYP3A4 и CYP2D6 в концентрациях, в 160 и 40 раз соответственно превышающих максимальные плазменные концентрации после приема дозы 20 мг. Более того, исследования лекарственного взаимодействия у людей показали, что лерканидипин не изменяет плазменные концентрации мидазолама, типичного субстрата CYP3A4, или метопролола, типичного субстрата CYP2D6. Поэтому ингибирования биотрансформации лекарственных средств, метаболизируемых с участием CYP3A4 и CYP2D6, при применении лерканидипина в терапевтических дозах не ожидается.
Выведение
Элиминация происходит в основном путем биотрансформации. Около 50% принятой дозы выводится почками. Среднее значение Т1/2 составляет 8-10 ч. Длительность терапевтического действия (24 ч) обусловлена связыванием лерканидипина с липидными мембранами. Кумуляции лерканидипина при повторном приеме внутрь не наблюдается.
Линейность/нелинейность фармакокинетики
Фармакокинетика лерканидипина в диапазоне терапевтических доз носит нелинейный характер. При приеме лерканидипина в дозах 10 мг, 20 мг и 40 мг Сmax в плазме крови определялась в соотношении 1:3:8 соответственно, и AUC – в соотношении 1:4:18, что предполагает прогрессирующее насыщение при «первом прохождении» через печень. Таким образом, биодоступность лерканидипина повышается с увеличением принятой дозы.
Фармакокинетика у особых групп пациентов
Пожилые пациенты. Было показано, что фармакокинетика лерканидипина у пожилых пациентов схожа с фармакокинетикой, которая наблюдается в общей популяции пациентов.
Нарушение функции почек. Было показано, что фармакокинетика лерканидипина, у пациентов с почечной недостаточностью легкой и средней степени тяжести (КК более 30 мл/мин) схожа с фармакокинетикой, которая наблюдается в общей популяции пациентов. У пациентов с тяжелой почечной недостаточностью (КК менее 12 мл/мин) и у пациентов, находящихся на гемодиализе, концентрации лерканидипина в плазме крови увеличивается примерно на 70%.
Нарушение функции печени. Было показано, что фармакокинетика лерканидипина у пациентов с печеночной недостаточностью легкой степени тяжести (класс А по классификации Чайлд-Пью) схожа с фармакокинетикой, которая наблюдается в общей популяции пациентов. У пациентов с печеночной недостаточностью (от средней до тяжелой) системная биодоступность лерканидипина, вероятно, увеличивается, поскольку лерканидипин метаболизируется главным образом в печени.
Показания препарата
Занидип®-Рекордати
- артериальная гипертензия I-II степени у взрослых пациентов.
Режим дозирования
Занидип®-Рекордати назначают внутрь 10 мг 1 раз/сут, как минимум, за 15 минут до еды, не разжевывая, запивая достаточным количеством воды. Препарат нельзя запивать грейпфрутовым соком.
Доза может быть увеличена до 20 мг в зависимости от антигипертензивной эффективности.
Увеличение дозы должно быть постепенным, поскольку до проявления максимального антигипертензивного эффекта может пройти около 2 недель.
Занидип®-Рекордати можно назначать в дополнение к бета-адреноблокаторам (атенолол), диуретикам (гидрохлоротиазид) или ингибиторам АПФ (каптоприл или эналаприл) в случае недостаточного эффекта от их применения.
Пациенты пожилого возраста: хотя фармакокинетические данные и клинический опыт свидетельствуют о том, что коррекции суточной дозы не требуется, начинать лечение у пожилых пациентов необходимо с осторожностью.
Пациенты детского возраста: безопасность и эффективность препарата Занидип®-Рекордати у детей и подростков в возрасте до 18 лет не изучалась.
Пациенты с нарушением функции почек или печени: следует проявлять особую осторожность при начале лечения пациентов с почечной или печеночной дисфункцией легкой или средней степени тяжести. Хотя обычные рекомендуемые схемы дозирования переносятся хорошо в этих подгруппах, к дозе до 20 мг/сут следует подходить с осторожностью. Антигипертензивный эффект может усиливаться у пациентов с нарушением функции печени, следовательно нужно рассмотреть необходимость коррекции дозы. Занидип®-Рекордати противопоказан пациентам с тяжелой печеночной недостаточностью или пациентам с тяжелой почечной недостаточностью (СКФ <30 мл/мин), включая пациентов, проходящих диализ (см. раздел «Противопоказания» и «Особые указания»).
Побочное действие
Обзор профиля безопасности
Безопасность лерканидипина в дозе 10-20 мг 1 раз/сут оценивалась в двойных слепых плацебо-контролируемых клинических исследованиях (группа лерканидипина — 1200 пациентов, группа плацебо — 603 пациента), а также в контролируемых и неконтролируемых продолжительных клинических исследованиях с участием в общей сложности 3676 пациентов с артериальной гипертензией. Наиболее частыми нежелательными реакциями в клинических исследованиях и при обобщении данных постмаркетингового опыта применения являются следующие: периферические отеки, головная боль, приливы, тахикардия и сердцебиение.
Нежелательные явления
В приведенной ниже таблице нежелательные реакции, зарегистрированные в клинических исследованиях и при обобщении данных постмаркетингового опыта применения, для которых существует обоснованная причинно-следственная связь, перечислены по классам систем органов MedDRA и частоте: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000), неизвестно (не поддается оценке по имеющимся данным). В каждой частотной группе нежелательные реакции представлены в порядке убывания серьезности.
1 Нежелательные реакции из спонтанных сообщений в мировом постмаркетинговом опыте.
Описание нежелательных реакций
В плацебо-контролируемых клинических исследованиях частота периферических отеков составила 0.9% при приеме лерканидипина в дозе 10-20 мг и 0.83% при приеме плацебо. Эта частота достигла 2% в общей популяции пациентов, включенных в клинические исследования, в т.ч. в долгосрочные.
Лерканидипин не влияет на концентрацию глюкозы и липидов плазмы крови.
Противопоказания к применению
- повышенная чувствительность к действующему веществу, другим производным дигидропиридинового ряда или любому из вспомогательных веществ;
- хроническая сердечная недостаточность в стадии декомпенсации;
- нестабильная стенокардия;
- обструкция выносящего тракта левого желудочка;
- острый инфаркт миокарда и период в течение 1 месяца после перенесенного инфаркта миокарда;
- тяжелая печеночная недостаточность;
- тяжелая почечная недостаточность (СКФ <30 мл/мин), включая пациентов, проходящих диализ;
- совместный прием со следующими препаратами:
- мощные ингибиторы CYP3A4,
- циклоспорин;
- совместный прием с грейпфрутом или грейпфрутовым соком;
- беременность;
- период грудного вскармливания;
- женщины детородного возраста, не пользующиеся надежными средствами контрацепции;
- детский возраст до 18 лет (эффективность и безопасность не изучались);
- дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция.
С осторожностью:
- синдром слабости синусового узла (без электрокардиостимулятора);
- дисфункция левого желудочка;
- ИБС;
- нарушения функции печени легкой и средней степени тяжести;
- нарушения функции почек легкой и средней степени тяжести;
- перитонеальный диализ;
- одновременный прием с индукторами/субстратами CYP3A4, мидазоламом, метопрололом, дигоксином;
- хроническая сердечная недостаточность;
- пожилой возраст.
Применение при беременности и кормлении грудью
Беременность
Данные о применении лерканидипина у беременных женщин отсутствуют. Исследования у животных не выявили тератогенных эффектов, но таковые наблюдались при применении других дигидропиридиновых производных. Применение лерканидипина противопоказано во время беременности и у женщин детородного возраста, не пользующихся надежной контрацепцией.
Грудное вскармливание
Поскольку нет данных об экскреции лерканидипина и его метаболитов в материнское молоко, риск для новорожденных и младенцев не может быть исключен. Лерканидипин противопоказан в период грудного вскармливания.
Фертильность
Клинические данные в отношении влияния лерканидипина на репродуктивную функцию отсутствуют. На фоне применения блокаторов медленных кальциевых каналов у единичных пациентов были зарегистрированы обратимые биохимические изменения в головке сперматозоидов, которые могут нарушать оплодотворение. В случаях, когда повторное экстракорпоральное оплодотворение безуспешно и когда невозможно найти другое объяснение, в качестве возможной причины следует рассмотреть применение блокаторов медленных кальциевых каналов.
Применение при нарушениях функции печени
Противопоказано применение препарата при тяжелой печеночной недостаточности.
С осторожностью следует назначать препарат при нарушениях функции печени легкой и средней степени.
Применение при нарушениях функции почек
Противопоказано применение препарата при тяжелой почечной недостаточности (СКФ <30 мл/мин), включая пациентов, проходящих диализ.
С осторожностью следует назначать препарат при нарушениях функции почек легкой и средней степени.
Применение у детей
Противопоказано применение препарата в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
С осторожностью следует назначать препарат пациентам пожилого возраста.
Особые указания
Синдром слабости синусового узла
У пациентов с синдромом слабости синусового узла (без электрокардиостимулятора) лерканидипин следует назначать с осторожностью.
Дисфункция левого желудочка
Хотя контролируемые исследования не выявили нарушений функции левого желудочка, необходимо проявлять осторожность у пациентов с уже существующей дисфункцией левого желудочка.
ИБС
Предполагается, что некоторые дигидропиридины короткого действия могут быть связаны с повышенным сердечно-сосудистым риском у пациентов с ИБС. Хотя лерканидипин обладает пролонгированным действием, при лечении таких пациентов необходимо проявлять осторожность. На фоне приема некоторых препаратов класса дигидропиридинов могут наблюдаться боли в грудной клетке по типу стенокардии. Очень редко у пациентов с уже существующей стенокардией может наблюдаться увеличение частоты, продолжительности или степени тяжести этих приступов. Могут наблюдаться единичные случаи развития инфаркта миокарда (см. раздел «Побочное действие»).
Аортальный стеноз/митральный стеноз/гипертрофическая обструктивная кардиомиопатия
Как и другие лекарственные средства, обладающие вазодилатирующим действием, лерканидипин следует с особой осторожностью применять у пациентов с аортальным стенозом, митральным стенозом или гипертрофической обструктивной кардиомиопатией. У пациентов с гемодинамически значимой обструкцией выносящего тракта левого желудочка (например, при тяжелом аортальном стенозе) применение лерканидипина противопоказано.
Хроническая сердечная недостаточность
У пациентов с хронической сердечной недостаточностью лерканидипин следует применять с особой осторожностью. До начала применения препарата необходимо достичь компенсации хронической сердечной недостаточности.
Нестабильная стенокардия/инфаркт миокарда
Опыт клинического применения лерканидипина при остром инфаркте миокарда и нестабильной стенокардии отсутствует, в связи с чем применение препарата при указанных заболеваниях противопоказано.
Применение при почечной или печеночной недостаточности
Следует проявлять особую осторожность в начале лечения у пациентов с нарушением функции почек легкой или средней степени тяжести. Хотя обычные рекомендуемые дозы 10 мг, как правило, пациенты переносят хорошо, к увеличению суточной дозы до 20 мг следует подходить с осторожностью.
Антигипертензивный эффект может усиливаться у пациентов с нарушением функции печени умеренной степени тяжести; следовательно, нужно рассмотреть необходимость коррекции дозы.
Лерканидипин противопоказан пациентам с тяжелой печеночной недостаточностью или тяжелой почечной недостаточностью (СКФ <30 мл/мин), а также пациентам, проходящим гемодиализ (см. раздел «Режим дозирования» и «Противопоказания»).
Перитонеальный диализ
У пациентов, находящихся на перитонеальном диализе, может наблюдаться мутный перитонеальный экссудат, что обусловлено повышенной концентрацией триглицеридов. Хотя механизм неизвестен, мутность экссудата имеет тенденцию разрешаться вскоре после отмены лерканидипина. Это важно помнить, т.к. мутный перитонеальный экссудат может быть ошибочно принят за один из симптомов инфекционного перитонита с последующей госпитализацией и эмпирическим введением антибиотиков.
Индукторы CYP3A4
Индукторы CYP3A4, такие как противосудорожные препараты (например, фенитоин, карбамазепин) и рифампицин, могут снижать концентрацию лерканидипина в плазме крови; следовательно, эффективность лерканидипина может быть снижена.
Алкоголь
Следует избегать употребления алкоголя, поскольку он может усиливать действие сосудорасширяющих антигипертензивных препаратов.
Лактоза
Препарат содержит лактозу, поэтому его применение у пациентов с редкой наследственной непереносимостью лактозы, дефицитом лактазы или синдромом глюкозо-галактозной мальабсорбции противопоказано.
Влияние на способность к управлению транспортными средствами и механизмами
Лерканидипин оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. Тем не менее, следует проявлять осторожность, поскольку на фоне приема могут возникать головокружение, астения, усталость и редко сонливость.
Передозировка
В постмаркетинговом опыте применения лерканидипина сообщалось о случаях передозировки в диапазоне от 30-40 мг до 800 мг, включая сообщения о попытке самоубийства.
Симптомы
Как и в случае с другими дигидропиридиновыми блокаторами медленных кальциевых каналов, передозировка лерканидипина приводит к чрезмерному расширению периферических сосудов с выраженной артериальной гипотензией и рефлекторной тахикардией. Однако при очень высоких дозах периферическая селективность может быть потеряна, с развитием брадикардии и отрицательного инотропного эффекта. Наиболее распространенными нежелательными реакциями, связанными со случаями передозировки, были артериальная гипотензия, головокружение, головная боль и сердцебиение.
Лечение
Клинически значимая артериальная гипотензия требует активной поддержки сердечно-сосудистой системы: мониторинг сердечной и дыхательной функции, возвышенное положение нижних конечностей, контроль ОЦК и диуреза. Ввиду длительного фармакологического эффекта лерканидипина важно, чтобы сердечно-сосудистый статус пациента с артериальной гипотензией контролировался как минимум в течение 24 ч. Поскольку препарат имеет высокую степень связывания с белками, диализ не эффективен. Пациенты с умеренной или тяжелой передозировкой должны наблюдаться в условиях отделения интенсивной терапии.
Лекарственное взаимодействие
Противопоказания к одновременному применению
Ингибиторы CYP3A4
Известно, что лерканидипин метаболизируется ферментом CYP3A4, и поэтому ингибиторы CYP3A4, применяемые одновременно, могут взаимодействовать с метаболизмом и элиминацией лерканидипина. Было показано, что одновременное применение с мощным ингибитором CYP3A4, кетоконазолом, повышает концентрацию лерканидипина в плазме крови (15-кратное увеличение AUC и 8-кратное увеличение Cmax для энантиомера S-лерканидипина).
Следует избегать одновременного назначения лерканидипина с ингибиторами CYP3A4 (например, кетоконазол, итраконазол, ритонавир, эритромицин, тролеандомицин, кларитромицин) (см. раздел «Противопоказания»).
Циклоспорин
После одновременного применения наблюдались повышенные концентрации в плазме крови как лерканидипина, так и циклоспорина. Исследование у молодых здоровых добровольцев показало, что при применении циклоспорина через 3 ч после приема лерканидипина плазменные концентрации лерканидипина не изменились, в то время как AUC циклоспорина повысилась на 27%. Однако совместное применение лерканидипина с циклоспорином вызвало 3-кратное увеличение концентраций лерканидипина в плазме крови и 21% повышение AUC циклоспорина.
Циклоспорин и лерканидипин не следует применять совместно (см. раздел «Противопоказания»).
Грейпфрут или грейпфрутовый сок
Лерканидипин не следует принимать с грейпфрутом или грейпфрутовым соком, т.к. одновременный прием может привести к увеличению системной доступности препарата и увеличению антигипертензивного эффекта (см. раздел «Противопоказания»).
Совместное применение не рекомендуется
Индукторы CYP3A4
К совместному применению лерканидипина с индукторами CYP3A4, такими как противосудорожные средства (например, фенитоин, фенобарбитал, карбамазепин) и рифампицин, следует подходить с осторожностью, поскольку антигипертензивный эффект может быть снижен, а контроль АД должен осуществляться в этом случае чаще, чем обычно (см. раздел «С осторожностью»).
Этанол (алкоголь)
При приеме сосудорасширяющих антигипертензивных препаратов следует избегать употребления алкоголя, поскольку он может усиливать их действие.
Меры предосторожности, включая коррекцию дозы
Субстраты CYP3A4
Следует соблюдать осторожность при одновременном назначении лерканидипина с другими субстратами CYP3A4, такими как терфенадин, астемизол, антиаритмические препараты класса III, такие как амиодарон, соталол (см. раздел «С осторожностью»).
Мидазолам
При одновременном назначении 20 мг мидазолама внутрь у пожилых добровольцев абсорбция лерканидипина увеличивалась (примерно на 40%), а скорость абсорбции снижалась (Tmax было отсрочено с 1.75 до 3 ч) (см. раздел «С осторожностью»). Концентрации мидазолама не изменялись.
Метопролол
При совместном приеме лерканидипина с метопрололом (бета-адреноблокатор, который в основном метаболизируется в печени), биодоступность метопролола не изменялась, тогда как биодоступность лерканидипина снижалась на 50%. Этот эффект может быть связан с уменьшением печеночного кровотока, вызванным бета-адреноблокаторами, и может встречаться при приеме других препаратов этого класса. Следовательно, лерканидипин можно безопасно применять с препаратами, блокирующими β-адренорецепторы, но может потребоваться коррекция дозы (см. раздел «С осторожностью»).
Дигоксин
При совместном применении лерканидипина (20 мг) с дигоксином не было выявлено признаков фармакокинетического взаимодействия. Однако наблюдалось среднее увеличение Cmax дигоксина на 33%, в то время как AUC и почечный клиренс изменялись незначительно. Таким образом, пациенты, получающие сопутствующее лечение дигоксином, должны находиться под наблюдением на предмет дигиталисной интоксикации (см. раздел «С осторожностью»).
Совместное применение с другими лекарственными средствами
Флуоксетин
Исследование взаимодействия с флуоксетином (ингибитором CYP2D6 и CYP3A4), проведенное у добровольцев в возрасте 65±7 лет (среднее значение ± СО), не выявило клинически значимых изменений фармакокинетики лерканидипина.
Циметидин
Одновременный прием циметидина (800 мг/сут) не вызывает значительных изменений концентрации лерканидипина в плазме крови, но при более высоких дозах необходимо проявлять осторожность, поскольку биодоступность и антигипертензивный эффект лерканидипина могут увеличиться.
Симвастатин
При повторном приеме дозы 20 мг лерканидипина совместно с 40 мг симвастатина AUC лерканидипина существенно не изменялась, в то время как AUC симвастатина увеличилась на 56%, а AUC его активного β-гидроксикилированного метаболита — на 28%. Маловероятно, что такие изменения имеют клиническое значение. Однако, когда прием лерканидипина переносят на утренние часы, а симвастатина на вечерние, лекарственного взаимодействия не наблюдается.
Варфарин
Совместное применение 20 мг лерканидипина у здоровых добровольцев натощак не изменяло фармакокинетику варфарина.
Диуретики и ингибиторы АПФ
Лерканидипин может одновременно применяться с диуретиками и ингибиторами АПФ.
Другие лекарственные препараты, влияющие на АД
Усиление антигипертензивного эффекта может наблюдаться при одновременном приеме лерканидипина с альфа-адреноблокаторами, трициклическими антидепрессантами, нейролептиками. Напротив, снижение антигипертензивного эффекта может наблюдаться при одновременном применении с ГКС.
Условия хранения препарата Занидип®-Рекордати
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Занидип®-Рекордати
Срок годности — 3 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
РУСФИК ООО, ГРУППА КОМПАНИЙ RECORDATI
(Россия)

|
|
РУСФИК ООО, 123610 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код